Cristales de cisplatino, un agente alquilante del grupo de los platinos.
Según el mecanismo de acción se clasifican básicamente de dos tipos, aquellos que actúan contra la célula tumoral en un determinado ciclo de la división celular denominados ciclo-específicos y aquellos ciclo-inespecífico que afectan a la célula durante todo su ciclo de desarrollo.
Muchos de los antineoplásicos son profármacos, es decir, se administra un medicamento que es menos tóxico, o tiene mejores características farmacodinámicas, y una vez en el organismo se convierte en otro fármaco más eficaz, seguro y selectivo frente a su diana terapéutica.
Índice
- 1 Clasificación de los antineoplásicos
- 2 Efectos secundarios de los citostáticos
- 3 Normas para la administración de citostáticos.
- 4 Véase también
- 5 Referencias
- 6 Enlaces externos
Clasificación de los antineoplásicos
Se realiza según el mecanismo de acción y dentro de éste según la estructura química del antineoplásico.Citostáticos que actúan sobre el ADN
1. Agentes alquilantes
Mostazas nitrogenadas
Ilustración de la estructura química de la ifosfamida.
porque es su principal efecto tóxico. También producen con frecuencia
vómitos y alopecia. Hay una complicación característica de la ciclofosfamida y de la ifosfamida, que es la cistitis hemorrágicas y se debe a la formación de un metabolito, la acroleína. En mayor grado la produce la ifosfamida.2 Esta cistitis hemorrágica se evita hidratando al paciente y usando MESNA (Uromitexan® amp) que es un protector de las células de la vejiga. Con la ifosfamida es obligatorio y con la ciclofosfamida no, aunque hay quien lo pone.
- Ciclofosfamida; Genoxal® amp, vial. Es muy útil por su amplio espectro combinado con otros fármacos en linfomas, leucemias, cáncer de mama y otros tumores sólidos.1
- Ifosfamida;
Tronoxal® vial. Se emplea sola o asociada en sarcomas (óseos o de
tejidos blandos), cáncer de ovario, de cérvix uterino y en cáncer de
pulmón entre otros. - Melfalan® comp., vial.
- Bendamustina, utilizada en el tratamiento de la leucemia linfática crónica y linfomas.
Nitrosoureas
En dosis altas pueden producir toxicidad pulmonar en forma de fibrosis. Tambien puede afectar en la orina.- Carmustina; Nitrourean® amp. Es muy lipófilo y alcanza fácilmente el SNC, por lo tanto se emplea en tumores cerebrales, enfermedad de Hodgkin.
2. Platinos
Ilustración tridimensional de la estructura química del cisplatino.
- Cisplatino.
Neoplatin®. Su reacción adversa más llamativa es la nefrotóxica y
produce náuseas y vómitos de gran intensidad. Se utiliza en cáncer de
células microcíticas de pulmón, estómago, testículo, ovario y linfoma de
no Hodgkin. - Carboplatino.
Paraplatin®. Produce menor nefrotoxicidad que el cisplatino pero
produce mayor mielotoxicidad, lo que va a limitar su dosis. Se utiliza
fundamentalmente en el cáncer avanzado de ovario. - Oxaliplatino. Eloxatin®. Se utiliza en el cáncer colorectal metastásico asociado al fluorouracilo (5-Fu).3
Produce menor nefrotoxicidad y hematotoxicidad que los anteriores, sin
embargo su neurotoxicidad, caracterizada por parestesia y disestesia
exacerbada o disparada por exposición a bajas temperaturas, limita su
dosis.
3. Antimetabolitos
Todos son depresores de la médula ósea.... y su toxicidad depende de la dosis y el tiempo de administración.4Análogos del ácido fólico
- Metotrexato® comp., iny. Su actividad se ve contrarrestada por la leucovorina o folinato cálcico, que se utiliza en la terapia de rescate. Produce mielosupresión, mucositis gastrointestinal y hepatitis. A dosis bajas se utiliza en la psoriasis, artritis reumatoide, leucemia linfocítica y cáncer de mama. También a dosis bajas en los embarazos ectópicos. A dosis altas se utiliza en el linfoma maligno. En este caso entra la terapia de rescate.
Análogos de la pirimidina
- Fluorouracilo®
comp., vial. Su reacción adversa más frecuente es sobre la médula ósea,
produce leucopenia, y también produce alteraciones gastrointestinales.
Se utiliza en cáncer de colon, mama, ovario. - capecitabina Administración oral. Utilizado para el tratamiento del cáncer de mama y el cáncer de colon.
- Citarabina® iny. Se emplea en el tratamiento de las leucemias.
- Gemcitabina.
Gemzar® iny. Se emplea en el cáncer de pulmón no microcítico
metastásico, en el carcinoma de páncreas y en el de vejiga, en este caso
se asocia a cisplatino.
Análogos de la purina
- Cladribina.
Leustatin® iny. Está indicada en el tratamiento de la tricoleucemia
activa y en la leucemia linfocítica crónica que no haya respondido a
otros tratamientos. Es un medicamento con elevada toxicidad. Las
alteraciones más graves que produce son hematológicas. - Mercaptopurina® comp. Se utiliza en distintos tipos de leucemia. Es útil en la enfermedad inflamatoria intestinal.
- Fludarabina.
Beneflur® iny. Se utiliza también en la leucemia linfocítica crónica
que no haya respondido a un tratamiento estándar con agentes
alquilantes. Produce neutropenia y trombocitopenia.
4. Antibióticos antitumorales
Ilustración de la comparación estructural entre la doxorubicina y epirubicina.
- Doxorubicina
o Adriamicina. Farmiblastina® iny. Se utiliza asociada con otros
antineoplásicos en leucemias, linfomas de Hodgkin y no Hodgkin, cáncer
de mama metastásico, de pulmón, etc.4 Existe una preparación comercial, Caelyx®, que es doxorubicina liposomal (en liposomas), que se emplea en el tratamiento del sarcoma de Kaposi en pacientes con sida. - Epirubicina.
Farmorubicina® iny. Se utiliza en linfomas malignos, carcinoma de
pulmón, mama, gástrico, hígado, páncreas, etc. El problema es que es
todavía más cardiotóxica que la doxorubicina.5 Tanto es así que no se deben aplicar dosis superiores a 1000mg/ porque aparece insuficiencia cardiaca congestiva. - Bleomicina. Bleomicina® iny. Produce unas reacciones características en la piel, como ulceraciones e hiperpigmentación. Se emplea en cáncer de testículo, enfermedad de Hodgkin y otros linfomas.6
- Mitomicina.
Mitomycin® iny. Tiene poco uso porque es muy tóxica. Produce náuseas,
vómitos, trombocitopenia e insuficiencia renal. Puede tener utilidad en
melanomas, cáncer de estómago y de páncreas. - Mitoxantrona. Novantrone® iny. Se utiliza en leucemias y linfomas no Hodgkin. También en cáncer de próstata
y hepatocelular. Sus efectos adversos más característicos son
cardiovasculares, gastrointestinales y hematológicos o sanguíneos.
5. Inhibidores de las topoisomerasas
Ilustración de la estructura química del Irinotecan.
- Irinotecan. Campto® iny (Topoisomerasa I).3 Se emplea en el cáncer colorrectal
avanzado combinado con 5-Fluorouracilo en pacientes sin quimioterapia
anterior o bien en monoterapia para pacientes que han fracasado a un
régimen anterior con 5-Fluorouracilo.3 Su principal reacción adversa son las diarreas. También puede producir síndrome colinérgico con calambres abdominales, bradicardia, hipersalivación, etc. Este síndrome puede evitarse si previamente se administra atropina. - Etoposido. Vepesid® cap, iny. (Topoisomerasa II).
Se utiliza en tumores testiculares, leucemias, cáncer microcítico de
pulmón y linfoma tanto Hodgkin como no Hodgkin. Produce mielodepresión, náuseas y vómitos. - Teniposido.
Vumon® iny. (Topoisomerasa II). Se emplea en algunos tipos de leucemias
y linfomas así como en los tumores intracraneales malignos.
6. Enzimas
- L- ASPARAGINASA. Kindrolase® (Med Extr). Produce reacciones de
hipersensibilidad, hipoalbuminemia y disminución de los factores de
coagulación. Se utiliza en el tratamiento de la leucemia linfoblástica
aguda en niños.
Fármacos que actúan sobre la mitosis celular sin afectar al ADN
1. Alcaloides de la vinca
pilosos. Son agentes vesicantes que provocan ulceraciones locales cuando
hay extravasación.
- Vinblastina.8 Como efecto adverso destaca la neurotoxicidad de carácter periférico y afecta también a la médula pero en menor medida.
- Vincristina.8 Vincrisul®. Produce mielodepresión en forma de leucopenia y también neurotoxicidad pero en menor medida.
- Vindesina. Enison®. Produce mielodepresión y neurotoxicidad pero más moderada.
- Vinorelbina.
Navelbine®. Se utiliza en el cáncer de pulmón de células no
microcíticas y en el carcinoma de mama avanzado. También produce
mielodepresión, neurotoxicidad y alopecia.
de linfomas y leucemias. La que más espectro tiene es la vindesina, que
se utiliza también en el cáncer colorectal, pulmonar, de mama, etc.
2. Taxanos
Producen leucopenia y neutropenia de corta duración y dan lugar con bastante frecuencia reacciones de hipersensibilidad.El paclitaxel
se utiliza en el cáncer de ovario asociado a cisplatino, en cáncer de
mama metastásico en pacientes que han fracasado o no son candidatos al
grupo de antraciclinas y en cáncer de pulmón no microcítico avanzado.9
El docetaxel sólo está indicado en el carcinoma de mama metastásico.9
Otros fármacos
Otros fármacos que se utilizan en los tumores malignos (sin ser antitumorales propiamente dichos).1. Agentes hormonales
- Antiestrogénicos
- Tamoxifeno® comp. Se utiliza en el cáncer de mama.
- Megestrol acetato. Megace® comp. Se utiliza en el cáncer de mama y en el de endometrio.
- Inhibidores de la aromatasa
- Aminoglutemida. Orimeten® comp. Carcinoma de mama y de próstata metastásico.
- Análogos de LH-RH
- Goserelina. Zoladex® iny. Cáncer de mama y próstata.
- Leuprolida. Procrin® iny. Cáncer de próstata.
- Antiandrogénicos
- Flutamida. Eulexin® comp. Cáncer de próstata.
- Ciproterona. Androcur® comp. Cáncer de próstata.
2. Sistema inmunitario
- Interleucinas. Promueven la proliferación de linfocitos T citotóxicos, linfocitos B y timocitos.
- Interferones. Como el α-2a y el α-2b, que intensifican la función de las células inmunológicas.
- Anticuerpos monoclonales. Como el Rituximab (Mabthera®), que se utiliza en el tratamiento de linfomas.
- Vacuna de la BCG. Son cepas atenuadas de Mycobacterium bovis. Se emplea en el cáncer de vejiga. Actúa a nivel local mediante la activación de macrófagos.
Efectos secundarios de los citostáticos
Manos de un paciente con eritrodisestesia palmo-plantar al cabo de 10 días con terapia antineoplásico.
una alteración en los mecanismos de control que regulan su capacidad de
diferenciación y proliferación. El tratamiento del tumor se puede
realizar mediante métodos quirúrgicos, radioterapia o fármacos
antineoplásicos o citostáticos.
En general, los citostáticos son más tóxicos para las células
tumorales que para las normales, por ser más activos sobre células en
fase de reproducción. Una de las principales características de los
tumores malignos es su continua división celular sin fases de reposo, lo
que los hace muy sensibles a los citostáticos. Sin embargo, algunas
células normales, como las de la médula ósea, las de la mucosa del
aparato digestivo o las células de los folículos pilosos se dividen
también con relativa rapidez por lo que son más sensibles a los
citostáticos.
El principal problema de estos fármacos es su elevada toxicidad
debido a la incapacidad para diferenciar las células tumorales de las
células sanas. Es muy frecuente administrar 2 ó 3 citostáticos juntos.
Estas asociaciones tienen la ventaja de que se pueden reducir la
resistencia de las células tumorales a los citostáticos y se puede
ampliar la potencia al emplear fármacos con diferente mecanismo de
acción. El inconveniente es que se pueden sumar los efectos tóxicos.
Para evitarlo se procura asociar citostáticos con distinta toxicidad.
La mayoría se administran por vía intravenosa y debido a que son muy
tóxicos es necesario ajustar la dosis con la mayor precisión posible. Se
ajusta por la superficie corporal que deriva del peso y talla. Se
administran normalmente en ciclos con períodos de descanso. Con estos
periodos de descanso se intenta que las células normales, por ejemplo
las de la médula ósea,
se recuperen del efecto tóxico del citostático mientras que las
tumorales se recuperan en menor cuantía. De esta forma y repitiendo los
ciclos se pretende reducir progresivamente el número de células
tumorales hasta conseguir su erradicación completamente mientras que las
células normales se mantienen al recuperarse después de cada ciclo.
Depresión de la médula ósea
Es uno de los más comunes y graves de muchos citostáticos. Aparecenprecozmente a los pocos días de tratamiento y es global ( hay anemia,
leucopenia y trombopenia).
Estas alteraciones se pueden paliar, por ejemplo:
- La anemia y la trombopenia se corrigen con transfusiones de hematíes y plaquetas.
- La leucopenia
mejora con los fármacos estimulantes de las colonias de granulocitos y
las complicaciones infecciosas secundarias a la leucopenia se tratan con
antibióticos y medidas de aislamiento.
Afectación de las mucosas del aparato digestivo.
Aunque se puede producir en cualquier zona, lo más frecuente es una intensa inflamación de la mucosa bucofaríngea (estomatitis o mucositis).Si se produce una mucositis son útiles los lavados con una solución de
anestésico local extremando las medidas higiénicas de la boca. También
suele aplicarse una solución de un antifúngico (Nistatina) para evitar la infección por Candida. Cuando se afecta la mucosa yeyunal puede haber diarrea y hemorragia digestiva.
Afectación de los folículos pilosos
Es frecuente la alopecia total que generalmente se resuelve al finalizar el tratamiento.Alteración de las gónadas
En las mujeres es frecuente la amenorreadurante la administración de citostáticos pero habitualmente se
recuperan los ciclos al interrumpir el tratamiento. En varones puede
producir [oligoespermia] y en algunos casos [esterilidad] permanente.
Los citostáticos pueden inducir malformaciones u otras enfermedades
congénitas, por eso durante el tratamiento y hasta 6 meses después se
debe evitar tener descendencia.
Vómitos
Para los cuales los antieméticos clásicos no suelen ser efectivos. El fármaco de elección es el Ondansetron y similares.Normas para la administración de citostáticos.
Preparación de las soluciones de citostáticos
La manipulación y preparación de estas soluciones entraña un riesgopara la persona encargada de realizarlas, especialmente si este es su
trabajo habitual, ya que estas soluciones son irritantes para la piel y
las mucosas y en algunos casos pueden absorberse lo suficiente como para
producir toxicidad general. Por lo tanto deben tomarse las siguientes
precauciones.
- Se preparan en una zona dedicada exclusivamente a ello, provista de
una campana de flujo laminar vertical. Esta cabina se ha de limpiar
diariamente con alcohol de 70 y semanalmente se hace una
descontaminación con una solución de pH básico.
- Se coloca un toalla estéril desechable, absorbente e impermeable en
la superficie de la campana para trabajar sobre ella y también se coloca
allí todo el material necesario para la manipulación (jeringas, sueros,
viales, etc.)
- El personal debe llevar una bata estéril impermeable, de un solo
uso, cerrada por delante y con puños elásticos. Se emplean también
guantes quirúrgicos de látex estériles que se colocan por debajo de los
puños de la bata. Estos guantes se deben cambiar cada hora como máximo y
en caso de rotura o contaminación. El gorro y la mascarilla son
opcionales excepto que no exista campana, entonces son obligatorios.
- Lavar cuidadosamente las manos antes de la colocación de los guantes y al terminar la preparación.
- Si el citostático se presenta en vial primero se desinfecta el tapón
con alcohol de 70, dejándolo evaporar. A continuación se introduce la
aguja con un ángulo de 45º con la superficie del tapón y el bisel hacia
arriba. Cuando haya penetrado la mitad del bisel entonces se coloca la
aguja perpendicularmente siguiendo una técnica que mantenga siempre una
presión negativa en el interior del vial. Se puede evitar la formación
de aerosoles con filtros de venteo.
- Si el citostático se presenta en una ampolla, antes de abrirla hay
que vigilar que no quede líquido en la parte superior. A continuación se
protege el cuello con una gasa estéril empapada en alcohol de 70. La
ampolla se ha de abrir en la dirección contraria a la del operador. Se
recomienda utilizar jeringas de tamaño adecuado porque no se debe ocupar
más de las ¾ partes de la capacidad.
- Debe existir un recipiente adecuado, que estará dentro de la
campana, para desechar los excesos de solución y todo el material
contaminado, que luego se incinera.
- En caso de exposiciones agudas se deben quitar y reemplazar
inmediatamente los guantes y las prendas contaminadas y luego lavar las
manos con abundante agua y jabón.
- Si nos ha afectado a alguna mucosa se lavará con solución salina (si afecta al ojo ir directamente al oftalmólogo).
- Las mujeres embarazadas no deben preparar citostáticos.
Infusión del citostático
La colocación de terapia intravenosa debe prepararse con las adecuadas condiciones de asepsia, especialmente en pacientes con infusiones continuas por varios días.
estos medicamentos debido a los riesgos que puede sufrir el paciente y a
la posibilidad de contaminación, tanto del ambiente como del
manipulador.
La infusión se hace a través de una cánula corta o de un catéter
largo. Lo más frecuente es canalizar una vena en cada tratamiento con
una cánula corta de teflón que se retira al terminar la infusión.
Hay que tomar una serie de precauciones:
- Extremar las medidas de asepsia porque estos enfermos en general tienen leucopenia y la inmunidad deprimida.
- Evitar las venas muy finas, inflamadas, en zonas con edemas o en zonas que hayan sido previamente radiadas.
- Asegurarse de que la cánula está bien situada en la vía venosa. Para
ello hay que llevar a cabo una prueba con una infusión de solución
salina, con el fin de comprobar que hay buen flujo y no hay escapes. El
retorno de sangre al aspirar es un dato deseable pero no siempre
garantiza que la cánula está bien colocada, especialmente si se han
hecho varios intentos para colocarla. En cada tratamiento de citostático
se debe cambiar de vena. - Para la expulsión de posibles burbujas en jeringa se debe colocar una gasa estéril alrededor e impregnada en alcohol.
- Si el citostático es en infusión siempre hay que vigilarlas. Al
finalizar la administración del citostático hay que lavar el equipo y la
vena con el suero de infusión. - Todo el material utilizado se debe depositar en envase adecuado para ellos con el rótulo “citostático”. Luego se incinera.
difícil obtener una vía venosa cada vez que hay que administrar se suele
insertar un catéter largo de teflón o silicona que permanece in situ
durante días, semanas o incluso meses. Al terminar la infusión del
citostático, el catéter se rellena con una solución de heparina y se
cierra. En algunos casos se usan catéteres cuyo extremo proximal termina
en un reservorio que se colocan subcutáneos.
Extravasación de soluciones de citostáticos
La extravasación, que es le instilación en el espacio perivascular deagentes citostáticos, es una de las complicaciones que puede ocurrir
durante la administración. Puede producir dolor prolongado, infección,
artritis (cuando la vena está sobre una articulación), necrosis de la
piel y tejido subcutáneo. Los citostáticos más peligrosos son los del
grupo de antibióticos y también los cuatro del grupo de la vinca. Todos
pueden producir necrosis extensas.
Aun así, casi todos los citostáticos producen molestias locales en el
punto de infusión con sensación de quemazón y calor que suele mejorar
con aplicación local de frío. Sólo una persona experta puede distinguir
estos síntomas con los de una extravasación, que son dolor, hinchazón de
la zona alrededor del punto o en sus inmediaciones. La comprobación de
la sospecha puede hacerse aspirando con una jeringa a través de la
cánula. Si no sale sangre hay extravasación. Si se produce, de deben
tomar las siguientes medidas:
- Detener la administración inmediatamente sin retirar la aguja e inmovilizar la extremidad.
- Intentar aspirar por la cánula con un a jeringa para recuperar parte de la solución extravasada.
- Aplicar medidas generales, como infiltrar 50-100 mg de
hidrocortisona o aplicar una pomada de hidrocortisona al 1% o bien
utilizar el antídoto específico según el citostático implicado. - Retirar la vía de administración y elevar la extremidad a nivel superior al corazón para mejorar el retorno venoso.
- Vigilar la evolución de la zona afectada, ya que a pesar de todas
las medidas se puede producir necrosis que a veces necesita los cuidados
de cirugía plástica.
Véase también
Referencias
- Fernández-Santander,
Ana; Armando Tejerina Gómez, Antonio Tejerina Bernal, Félix Gómez
Gallego, Catalina Santiago Dorrego y Fernando Bandrés Moya. Aspectos Farmacogenéticos en el tratamiento del cáncer de mama con tamoxifeno. Fundación Tejerina. pp. 45–50. ISBN 8493546860.
Enlaces externos
- Fármacos antineoplásicos Departamento de Farmacología y Terapéutica - Facultad de Medicina: Universidad Autónoma de Madrid.
(artículo completo disponible en español). Rev Panam Salud Publica
[online]. 1998, vol.4, n.4 [cited 2010-01-06]. ISSN 1020-4989. doi:
10.1590/S1020-49891998001000013.
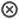









No hay comentarios:
Publicar un comentario